Nghiên cứu tăng cường enzyme làm thoái hóa nhựa
Người Brazil tham gia vào dự án quốc tế để tăng cường năng lực của PETase trong việc phá vỡ polyetylen terephthalate (PET), được sử dụng trong chai và chịu trách nhiệm sản xuất hàng triệu tấn chất thải.
Người Brazil tham gia vào dự án quốc tế để tăng cường năng lực của PETase trong việc phá vỡ polyetylen terephthalate (PET), được sử dụng trong chai và chịu trách nhiệm sản xuất hàng triệu tấn chất thải.
Link:
http://www.pnas.org/content/early/2018/04/16/1718804115
http://www.bv.fapesp.br/en/pesquisador/85580/rodrigo-leandro-silveira
http://www.bv.fapesp.br/en/pesquisador/2269/munir-salomao-skaf
http://cepid.fapesp.br/en/centro/13
http://cepid.fapesp.br/en/home
http://www.lnls.cnpem.br/sirius-en
Kể từ khi được phát hiện, enzyme có tên là PETase đã thu hút rất nhiều sự quan tâm của giới khoa học đối với khả năng tiêu hóa PET (polyethylen terephthalate). Một loại polymer được sử dụng chủ yếu để sản xuất chai nước uống (nhưng cả quần áo, thảm và các vật thể khác), PET được ngành công nghiệp đánh giá cao vì lý do tương tự khiến PET trở thành mối đe dọa cho môi trường: khả năng chống suy thoái. Chai và các vật thể khác làm bằng nhựa PET (polyethylen terephthalate) phải mất ít nhất 800 năm để phân hủy sinh học trong các bãi chôn lấp hoặc trên biển. Từ 4,8 tỷ đến 12,7 tỷ kg nhựa được đổ ra đại dương mỗi năm
Một nghiên cứu với kết quả được công bố gần đây trên tạp chí Proceedings of the National Academy of Science of America (PNAS) đã chỉ ra cách một nhóm cộng tác viên quốc tế quản lý để tăng cường năng lực của PETase để phá vỡ nhựa.
"Trong dự án nghiên cứu của chúng tôi, chúng tôi đã mô tả cấu trúc ba chiều của enzyme có thể tiêu hóa loại nhựa này, chế tạo nó để tăng khả năng phân hủy và chứng minh rằng nó cũng hoạt động trên polyetylen-2,5-furandicarboxylate (PEF), một loại nhựa PET Rodrigo Leandro Silveira, một nghiên cứu sinh sau tiến sĩ tại Viện Hóa học của Đại học Campinas (IQ-UNICAMP), được hỗ trợ bởi Quỹ nghiên cứu São Paulo - FAPESP, người đồng ký kết bài báo.
Cũng được liệt kê là đồng tác giả là các nhà khoa học từ Đại học Portsmouth (Anh) và từ Phòng thí nghiệm năng lượng tái tạo quốc gia Hoa Kỳ, những người hợp tác trong nghiên cứu, cũng như giám sát viên của Silveira, Munir Salomão Skaf. Một giáo sư đầy đủ tại UNICAMP và cũng là Hiệu trưởng nghiên cứu của nó, Skaf điều hành Trung tâm khoa học kỹ thuật và tính toán (CCES) - một trong những Trung tâm nghiên cứu, đổi mới và phổ biến (FIDES) của FAPESP - cũng cung cấp kinh phí cho nghiên cứu.
Sự quan tâm đến PETase đã tăng lên vào năm 2016, khi một nhóm các nhà nghiên cứu Nhật Bản do Shosuke Yoshida dẫn đầu đã xác định được một loài vi khuẩn mới, Ideonella sakaiensis, có thể "nuôi" PET bằng cách sử dụng nó làm nguồn carbon và năng lượng. Vi khuẩn vẫn là sinh vật duy nhất được biết đến với khả năng này. Nó thực sự phát triển trên PET.
Bên cạnh việc xác định I. sakaiensis, các nhà khoa học Nhật Bản phát hiện ra rằng nó tạo ra hai loại enzyme và tiết ra chúng vào môi trường", Silveira giải thích. "Một trong những enzyme được tiết ra chính xác là PETase. Vì nó có độ tinh thể nhất định, PET là một loại polymer rất khó phân hủy. Nhưng PETase tấn công nó và phá vỡ nó thành các đơn vị nhỏ axit terephthalic mono (2-hydroxyethyl) hoặc MHET. Các đơn vị của MHET sau đó được chuyển thành axit terephthalic và được vi khuẩn hấp thụ và chuyển hóa. "
I. Sakaiensis là loài sống duy nhất được biết đến với việc không sử dụng các phân tử sinh học, mà là một phân tử tổng hợp được sản xuất bởi con người để tồn tại. Điều này có nghĩa là vi khuẩn là kết quả của một quá trình tiến hóa rất gần đây đã diễn ra trong vài thập kỷ qua. Vi khuẩn này đã thích nghi với một loại polymer được phát triển vào đầu những năm 1940 và chỉ bắt đầu được sử dụng ở quy mô công nghiệp vào những năm 1970. PETase là chìa khóa để hiểu làm thế nào.
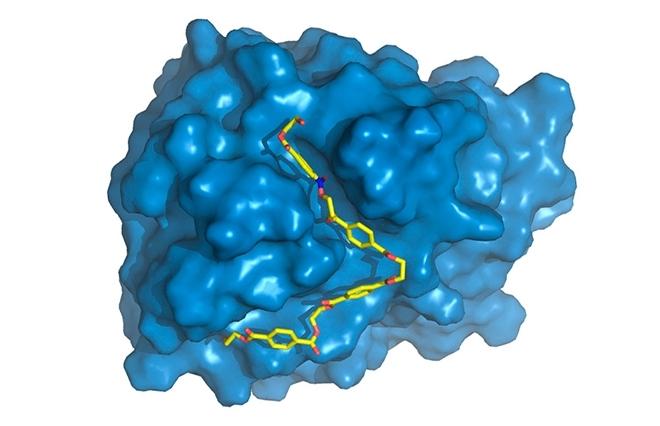
"PETase thực hiện phần khó nhất, đó là phá vỡ cấu trúc tinh thể và làm mất hoạt tính của PET thành MHET," nhà nghiên cứu do FAPESP tài trợ cho biết. "Công việc được thực hiện bởi enzyme thứ hai, biến MHET thành axit terephthalic, đơn giản hơn nhiều, vì cơ chất của nó bao gồm các monome mà enzyme có thể truy cập dễ dàng vì chúng phân tán trong môi trường phản ứng. Vì lý do này, nghiên cứu đã tập trung vào nghiên cứu. trên PETase. " Bước tiếp theo là nghiên cứu chi tiết về PETase, và đây là đóng góp của dự án nghiên cứu mới. "Chúng tôi tập trung vào việc tìm ra những gì mang lại cho PETase khả năng làm một thứ mà các enzyme khác không thể làm rất hiệu quả. Chúng tôi đã bắt đầu bằng cách mô tả cấu trúc 3D của protein này", Silveira giải thích. "Có được cấu trúc 3D có nghĩa là khám phá tọa độ x, y và z của mỗi trong số hàng ngàn nguyên tử bao gồm đại phân tử. Các đồng nghiệp người Anh của chúng tôi đã làm điều này bằng cách sử dụng một kỹ thuật nổi tiếng và được sử dụng rộng rãi gọi là nhiễu xạ tia X có sẵn trong phòng thí nghiệm tương tự như Sirius, hiện đang được xây dựng ở Campinas. "
Khi họ đã có được cấu trúc 3D, các nhà nghiên cứu bắt đầu so sánh PETase với các protein liên quan. Họ hàng gần nhất là một cutinase của vi khuẩn Thermobifida fusca làm thoái hóa cutin, một loại vecni tự nhiên được tìm thấy trên lá của cây. Một số vi sinh vật gây bệnh sử dụng cutinase để phá vỡ hàng rào cutin và các chất dinh dưỡng thích hợp trong lá.
"Chúng tôi đã tìm thấy một số khác biệt cụ thể về PETase so với cutinase trong khu vực của enzyme nơi xảy ra các phản ứng hóa học, được gọi là vị trí hoạt động. Ví dụ, PETase có một vị trí hoạt động cởi mở hơn", Silveira nói. "Chúng tôi đã nghiên cứu chuyển động phân tử của enzyme thông qua mô phỏng máy tính, phần mà tôi đóng góp nhiều nhất. Trong khi cấu trúc tinh thể, thu được từ nhiễu xạ tia X, cung cấp thông tin tĩnh, mô phỏng cho chúng tôi thông tin động và cho phép chúng tôi khám phá vai trò cụ thể của từng loại amino axit trong quá trình phân hủy PET. "
Vật lý của các chuyển động của phân tử là kết quả của lực hút tĩnh điện và lực đẩy của rất nhiều nguyên tử và từ nhiệt độ. Mô phỏng máy tính cho phép các nhà nghiên cứu hiểu hoàn toàn hơn về cách thức PETase liên kết và tương tác với PET.
"Chúng tôi đã phát hiện ra rằng PETase và cutinase có hai axit amin khác nhau tại vị trí hoạt động. Sau đó, chúng tôi đã sử dụng các quy trình sinh học phân tử để tạo đột biến trong PETase với mục đích chuyển đổi nó thành cutinase", Silveira nói.
"Nếu chúng tôi có thể làm điều đó, chúng tôi sẽ chỉ ra lý do tại sao PETase là PETase. Nói cách khác, chúng tôi sẽ tìm ra thành phần nào mang lại cho nó tính chất độc nhất của việc khử PET. Tuy nhiên, thật ngạc nhiên, khi chúng tôi cố gắng ngăn chặn hoạt động đặc biệt này của PETase - bằng cách chuyển đổi PETase thành cutinase - chúng tôi đã tạo ra một PETase hoạt động mạnh mẽ hơn nữa. Chúng tôi đã cố gắng giảm hoạt động của nó, và thay vào đó chúng tôi đã thúc đẩy nó. "
Cần nhiều mô phỏng máy tính hơn để hiểu tại sao PETase đột biến lại tốt hơn PETase gốc. Mô hình hóa và mô phỏng rõ ràng cho thấy rằng những thay đổi được tạo ra trong PETase ban đầu đã tạo điều kiện cho enzyme liên kết với cơ chất.
Liên kết này phụ thuộc cả vào hình học, với hai phân tử khớp với nhau như chìa khóa và lỗ khóa và vào các yếu tố nhiệt động liên quan đến sự tương tác giữa các thành phần khác nhau của enzyme và polymer. Cách thanh lịch để mô tả điều này là PETase biến đổi có "ái lực lớn hơn" với chất nền.
Xét về một ứng dụng thực tế trong tương lai, để có được một thành phần có thể tiêu hóa hàng tấn chất thải nhựa, nghiên cứu đã thành công lớn, nhưng tại sao PETase là PETase vẫn là một bí ẩn.

